|
Местный
Регистрация: 07.05.2024
Сообщений: 560
Спасибо: 0
Спасибо 3 в 3 постах
Репутация: 10
|
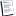
Старение и инсулиновый каскад.
Влияние опосредуемого инсулином и IGF-1 сигнального механизма на продолжительность жизни сохранились в ходе эволюции. Системное подавление этого механизма, также как и избирательная стимуляция активности фактора транскрипции FOXO (аналога DAF-16) в жировой ткани продлевает жизнь мух-дрозофил. У инбредных линий мышей также обнаружена выраженная обратная взаимосвязь между уровнем IGF-1 и продолжительностью жизни. Аналогичным эффектом обладают также мутации, подавляющие активность рецепторов к инсулину и IGF-1, а также других белков-участников сигнального механизма. Схожая взаимосвязь наблюдается и у собак. Существуют данные, согласно которым собаки низкорослых пород, имеющие мутацию, снижающую активность IGF-1, живут дольше крупных собак. Однако для мух-дрозофил и мышей существование взаимосвязи между размером тела и продолжительностью жизни не подтвердилась.
https://3.bp.blogspot.com/-X68pIGOi4Yg/V54oDzpW3iI/AAAAAAAAL4Y/okFUDnILr7w14Y4pCWMxzYgIPdz5cgCxQCLcB/s400/02.IIS-i-mTOR.png
Доказательства влияния ИФР1 каскада на продолжительность жизни были показаны на различных моделях млекопитающих. Хорошим примером могут быть карликовые мутантные мыши, дефицитные по гормону роста. Такие мыши не только долго живут, у них замедленно старение иммунной системы (клеточное старение), перекрестные сшивки коллагена, замедлено старение летальных заболеваний и случайных патологических процессов, таких как артриты. Также, у грызунов, которых посадили на диету (ограниченное питание), наблюдалось снижение уровня инсулина и ИФР1. Снижалось количество запасаемого жира, стимулировалась иммунная система. Продолжительность жизни возрастала на 30-40 %. Генетические модели также показали влияние ИФР1 каскада на продолжительность жизни.
В 2009 году было проведено исследование на группе пожилых европеоидов. Исследовали 30 генов insulin/ИФР1-сигнального пути. В ходе этого исследования были найдены SNP, достоверно связанные с продолжительностью жизни. Один из этих SNP был найден в гене AKT1. И еще две SNP в гене FOXO3A были связаны с продолжительностью жизни у женщин. Для человека важную роль играет соотношение ГР/ИФР1. При относительно большом количестве гормона роста (при недостатке ИФР1) могут развиться такие симптомы, как ожирение, умственная отсталость, непереносимость глюкозы (синдром Ларона)
По аналогии с другими животными, у млекопитающих ИФР1-каскад негативно регулирует факторы трансляции генов FOXO. FOXO — это сильно консервативное у млекопитающих семейство генов, необходимых для выживания организма в стрессовых условиях. Более того, при редукции ИФР1 сигнала у мышей наблюдалась большая устойчивость к оксидативному стрессу. Таким образом, на мышах, моделированных для изучения болезни Альцгеймера, было показано комплексное влияние ИФР1-каскада на защитные системы организма.
Инсулиновый каскад и раковые болезни.
Путь ИФР сигнализации имеет патогенную роль в развитии рака. Исследования показали, что при повышенном уровне ИФР усиливается рост раковых клеток. Увеличение уровня ИФР-1 связано с повышенным риском возникновения основных типов рака, включая рак толстой кишки, молочной железы и простаты. Такие виды рака стимулируют митоз (деление клеток) и задерживают апоптоз (процесс отмирания клеток). Это значит, что ИФР-1 не только способствует распространению раковых клеток, но также не дает иммунной системе идентифицировать и уничтожить аномальные клетки до того, как они станут раковыми (то есть препятствует возникновению апоптоза).
Более того, по мере нашего старения высокая циркуляция уровня ИФР-1 способствует делению поврежденных клеток, которые в противном случае не стали бы злокачественными. Повышенный уровень ИФР-1 также способствует росту и пролиферации клеток опухоли и повышает их выживаемость, адгезию, миграцию, степень проникновения, ангиогенез и метастатический рост. Сокращение уровня ИФР-1 у взрослых вызывает сокращение окислительного стресса, уменьшение воспалений, улучшение чувствительности к инсулину и увеличивает продолжительность жизни.
По данным Европейского проспективного исследования раковых заболеваний и питания установлено, что повышенный уровень ИФР-1 увеличивает на 40 % риск развития рака груди у женщин старше пятидесяти лет. Другими словами, высокий уровень ИФР-1 способствует появлению распространенных типов рака и провоцирует появление слабоумия, в то время как низкий уровень ИФР-1 позволяет поддерживать работу мозга в пожилом возрасте.
Повышенное содержание ИФР-1 было обнаружено у пациентов с болезнью Альцгеймера, а его уменьшение снижало симптоматику этого заболевания. В случае мышечных тканей, которым в пожилом возрасте требуется ИФР-1 для правильной работы и восстановления, локальное производство ИФР-1 за счет мускульного напряжения хватает для поддержания ИФР-1 на нижних уровнях допустимых показателей. Так что низкий уровень инсулиноподобного фактора роста у взрослых людей способствует долголетию и не имеет никаких очевидных недостатков.
Хороший ИФР-1.
Как и у любой медали есть 2 стороны, так и много хорошего есть и у ИФР-1. Способность к росту важна для обновления и репарации клеток. ИФР-1 важен для многих функций гормона роста, стимулирует рост костей и других тканей организма, а также способствует увеличению мышечной массы. Гормон роста и ИФР-1 стимулируют пролиферацию эндотелиальных клеток сосудистой стенки, ангиогенез в целом, репарацию нервной ткани, утилизацию глюкозы клетками мозга.
Снижением продукции СТГ и ИФР-1 обусловлены такие старческие изменения, как ухудшение внутриклеточного синтеза белка, дистрофические изменения кожи, потеря костной массы, когнитивные нарушения, иммунодепрессия, сосудистая недостаточность. Старение характеризуется нарушением репаративных процессов. Клетки, неспособные к репарации, получают команду к запрещению деления, а при критической массе повреждений — к массовому *******йству клеток в жизненно важных органах. Но активность ИФР-1 необходимо ограничивать, чтобы не проявлялись ее негативные свойства.
Гиперинсулинемия и раковые заболевания.
Чем меньше у человека чувствительность к инсулину, тем более высокий уровень этого гормона у него будет вырабатываться.
Многоголовая гидра: метаболический синдром и болезни цивилизации.
Это состояние называется нарушенная толерантность к глюкозе. У больных с СД2 (сахарным диабетом) и абдоминальным ожирением изменение чувствительности к инсулину и некоторые другие приобретают патологический характер, соответственно, увеличивается риск развития онкозаболеваний. В настоящее время доказано, что у лиц, страдающих СД, риск таких злокачественных новообразований, как рак печени, поджелудочной железы, колоректальный рак и рак тела матки значительно выше, чем в популяции в целом. Относительно рака молочной железы, яичника, почек мнения исследователей расходятся.
По ряду данных, нарушенная толерантность к глюкозе более опасна как фактор онкологического риска, чем манифестный СД2. Частота злокачественных новообразований у больных с СД2 выше, чем при гестационном диабете; а у больных с гестационным диабетом она выше, чем при СД 1. Такая закономерность отражает патогенетическую связь неопластических процессов со степенью гиперинсулинемии. Как подтвердило 5-летнее проспективное наблюдение, при одной и той же локализации карцином риск рецидивов и смерти повышен у больных с гиперинсулинемией. Гиперинсулинемия способствует также злокачественному течению рака предстательной железы.
Вышеприведенные данные указывают на вероятность связи между риском возникновения злока-чественных новообразований и экспрессией генов, ассоциированных с продукцией инсулина и чувствительностью к нему периферических рецепторов (например, генов рецепторов лептина, фактора некроза опухоли, ИЛ-6 и т.д.).
Повышенная секреция инсулина у больных с СД2 и ожирением вызывает увеличение уровня ИФР-1, стимулирующего усиленное деление клеток. Важно учитывать также, что гиперинсулинизм в патогенезе СД2 сопровождается гипергликемией, образованием конечных продуктов гликирования и активных форм кислорода. Активные формы кислорода способны повреждать цитоплазматические и митохондриальные мембраны, влиять на утрату теломер, снижать интенсивность репарации ДНК и в связи с этим — на угасание способности клеток к воспроизводству.
|